Accueil Arborescence Page précédente

|
Modèle de Bohr
La petite histoire Comprendre simplement Domaines de présence Son interprétation dans l'avenir Les références Mais encore |
|
by Pepe © Accueil Arborescence Page précédente |

|
|
La petite histoire Up Page Origine, raisons, hasard 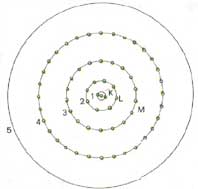 Le modèle atomique est de plus en plus raffiné.
Thomson a découvert l'électron, Rutherford a
identifié le proton et Bohr a
déterminé l'emplacement des électrons
autour du noyau. Une autre énigme reste à
solutionner dans le modèle atomique: Comment les protons
chargés positivement surmontent-ils la force de
répulsion électrique qui devrait normalement les
éloigner les uns des autres et provoquer
l'éclatement du noyau?
Le modèle atomique est de plus en plus raffiné.
Thomson a découvert l'électron, Rutherford a
identifié le proton et Bohr a
déterminé l'emplacement des électrons
autour du noyau. Une autre énigme reste à
solutionner dans le modèle atomique: Comment les protons
chargés positivement surmontent-ils la force de
répulsion électrique qui devrait normalement les
éloigner les uns des autres et provoquer
l'éclatement du noyau?
|
|
Comprendre simplement Up Page Energie de l'atome quantifié  Planck postule que les échanges d'énergie entre
la matière et les ondes
électromagnétiques sont quantifiés.
Planck postule que les échanges d'énergie entre
la matière et les ondes
électromagnétiques sont quantifiés. Einstein associe les photons aux quanta de Planck, élabore la théorie de la relativité et énonce la formule d'équivalence de la masse et de l'énergie. Bohr perfectionne le modèle planétaire de l'atome et donne une interprétation du spectre de l'hydrogène en postulant que l'énergie de l'atome est quantifiée. |
|
Domaines de présence Up Page Rayonnement électromagnétique à chaque saut orbital La théorie de Bohr sur la structure atomique, pour laquelle il reçut le prix Nobel de physique en 1922, fut publiée entre 1913 et 1915. Son travail s'inspira du modèle nucléaire de l'atome de Rutherford, dans lequel l'atome est considéré comme un noyau compact entouré d'un essaim d'électrons. Bohr ne pouvait expliquer pourquoi les électrons en mouvement autour du noyau ne s'écrasaient pas sur le noyau, ce qui aurait provoqué une destruction de l'atome. Il ne comprenait pas pourquoi les atomes d'un même élément, si ses électrons gravitaient à des endroits différents, pouvaient tous réagir de la même façon chimiquement. De plus, selon les lois de la physique classique, une charge électrique (électron) en mouvement dans un champ électromagnétique devrait irradier de la lumière ou une autre forme d'énergie et ainsi perdre toute son énergie. Pour solutionner cette problématique capitale, Bohr est parti du principe que l'atome n'émet de rayonnement électromagnétique que lorsqu'un électron se déplace d'un niveau quantique à un autre. Pour appuyer son postulat, il s'est servi de la théorie quantique et la constante de Planck (le rapport entre la taille du quantum et la fréquence du rayonnement); la théorie du quantum de Max Planck, énoncée en 1901. |
|
Son interprétation dans l'avenir Up Page Répartition des électron autour du noyau En analysant les atomes d'hydrogène (l'hydrogène ne possède qu'un électron) excités dans un tube cathodique, il remarque que ceux-ci émettent une lumière caractéristique qu'un prisme décompose en bandes de lumière appelées spectre de raies. Comme chacune de ces raies possèdent une énergie spécifique, Bohr décide d'associer chacune d'elles à une couche sur laquelle peuvent se retrouver les électrons. Lorsque l'atome est excité par un "paquet" d'énergie extérieure, l'électron passe alors à un niveau d'énergie supérieure et ce, d'un seul bond, car l'électron ne peut se trouver entre deux niveaux. Lorsque les électrons reviennent à leur état fondamental ou stationnaire (le plus près du noyau), ils perdent le même "paquet" d'énergie qu'ils ont reçu sous forme de lumière. En 1914, à partir de sa théorie du spectre d'émission de l'hydrogène, Bohr propose son modèle atomique en modifiant celui de Rutherford. Il situe les électrons sur des orbites particulières nommées couches électroniques ou niveaux énergétiques. L'énergie d'un électron sur sa couche électronique fondamentale est constante. Par conséquent, il n'y a aucune énergie émise lorsque l'électron est sur cette couche stationnaire, donc il n'y a pas de perte d'énergie. Le nombre maximum d'électrons sur une couche électronique est donné par la formule 2 n² où n égale le nombre de couches. Ainsi, la première couche ne peut recevoir que deux électrons, alors que les autres couches en recevront huit ou davantage. Actuellement, sept niveaux d'énergie suffisent pour représenter les éléments du tableau périodique. La dernière couche électronique d'un atome de possède jamais plus de 8 électrons. Les atomes sont plus stables lorsque leur couche extérieure est remplie; ils tendent vers cette stabilité en participant à des réactions chimiques au cours desquelles ils gagnent, perdent ou partagent des électrons. Le modèle de Bohr explique maintenant le comportement et la distribution des électrons autour du noyau de l'atome. Malheureusement, il ne permet pas de décrire avec succès les spectres des atomes polyélectroniques. |
|
Les références Up Page Réseau Pepe Chat de Schrödinger John Gribbin Initiations à la physique Max Planck Physique nouvelle et les quanta Louis de Broglie Pourquoi ce site Je crois que, si les êtres humains que nous sommes ne parviennent pas toujours à évoluer comme ils le souhaiteraient _à s'épanouir professionnellement, sentimentalement et sexuellement (ce que j'appelle les trois pôles d'intérêts) c'est parce qu'il y a des barrages qui entravent leur désir d'accéder à un rêve inachevé. Je pars du principe que tout est possible, à condition de s'entourer de gens qui nous poussent à croire en nous. Contribuer au Réseau Pepe Ce site est avant tout une encyclopédie ouverte à l'imagination et au savoir, où chacun(e) d'entre vous peut participer. Si vous avez envie de partager une passion, ou si vous sentez le besoin de vous exprimer sur un point précis, je vous invite à m'adresser un e-mail (adresse électronique accessible sur ma page d'accueil). |
|
Mais encore Up Page Ce que vous avez toujours voulu savoir Le mystère s'éclaircit. Toutefois, il reste encore celui des protons. Comment surmontent-ils la force de répulsion électrique qui devrait normalement les éloigner les uns des autres et provoquer l'éclatement du noyau? James Chadwick répondra à cet énigme en découvrant une nouvelle particule dans le noyau de l'atome. |